-高雄醫學大學 研發處-
ICB免疫療法的兩大挑戰:副作用與MHC限制性
免疫檢查點抑制劑(Immune checkpoint inhibitors, ICB)是一項改變癌症治療方式的突破性策略,透過阻斷像是CTLA-4、PD-1或PD-L1這些抑制T細胞功能的分子,重新喚醒免疫系統來對抗癌細胞[1-5]。雖然這類療法在黑色素瘤和肺癌等多種癌症中都有不錯的效果,但仍存在不少挑戰。其中最明顯的問題之一,就是ICB藥物常引起強烈副作用。以CTLA-4抑制劑Yervoy為例,雖然它可以有效激活免疫反應,但也可能導致全身性免疫過度活化,產生如腸膜炎、肝炎、內分泌失調、皮膚毒性,甚至神經發炎等嚴重副作用[6-9]。這些反應有時嚴重到需要停藥,甚至影響病人的生活品質與預後,因此,提升ICB抗體在腫瘤區域的選擇性,成為當務之急。
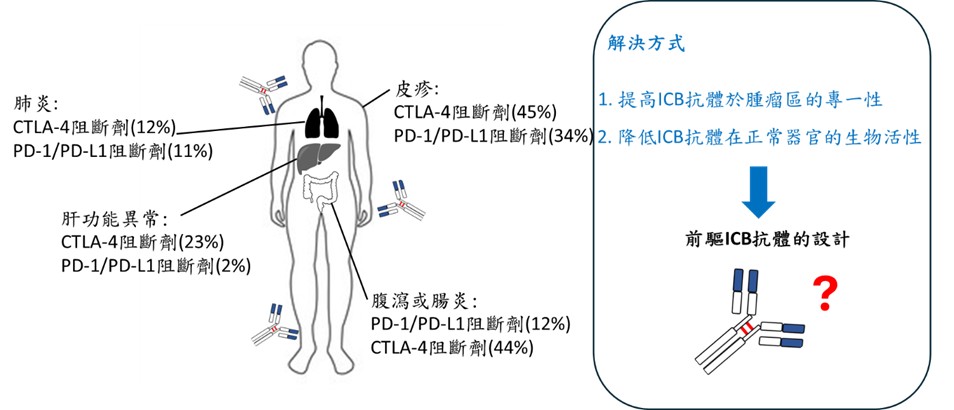
另一個限制療效的因素是腫瘤對免疫系統的「隱身術」——也就是腫瘤細胞表現的MHC I分子(主要組織相容性複合體)不足。MHC I 是T細胞辨識腫瘤抗原的重要關鍵,但許多腫瘤會主動降低MHC I的表現,進而逃避免疫攻擊。研究發現,像是缺乏Beta-2-microglobulin(MHC I 組成的關鍵元件)的黑色素瘤病人,對Yervoy的反應率明顯降低(約只有正常病人的1/4),整體預後也比較差。總結來說,免疫檢查點抑制劑目前在臨床應用上仍面臨兩大挑戰:第一,缺乏組織選擇性導致嚴重副作用;第二,腫瘤MHC分子表現不足,導致療效受限。為了解決這些問題,科學界正積極尋求更安全、更具靶向性的解方。
我們的解法:打造專一性更高的IFNγ-Yervoy融合抗體
為了解決上述挑戰,我們團隊開發了一種具腫瘤選擇性的「前驅型干擾素-Yervoy融合抗體」(IFNγ-Yervoy),目的是同時解決ICB副作用大與腫瘤MHC表現不足的兩個難題。這項新策略的關鍵設計是結合一段MMP-2專一性酵素裂解序列,把干擾素(IFNγ)與免疫檢查點抑制劑Yervoy(Ipilimumab, anti-CTLA-4)連結起來。這樣的設計讓這個融合抗體在血液與正常組織中處於「沉睡狀態」,不會主動發揮免疫功能;但一旦進入腫瘤區域、遇到高度活化的MMP-2/9酵素時,就會被切割釋放,讓IFNγ與Yervoy重新啟動功能。
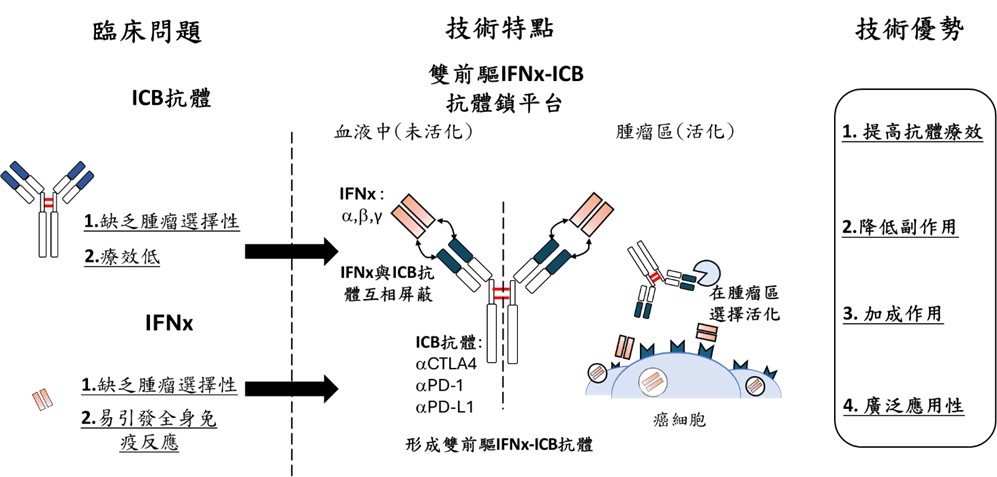
這個平台的運作就像是雙保險:Yervoy負責阻斷CTLA-4、進而活化T細胞;IFNγ則能提升腫瘤細胞的MHC I 表現,讓免疫系統更容易辨識並攻擊腫瘤。兩者協同作用下,不只能提升療效,還能大幅降低全身副作用,實現真正「對腫瘤有效、對正常組織友善」的癌症免疫治療。
我們的創新解法:IFNγ-Yervoy融合抗體
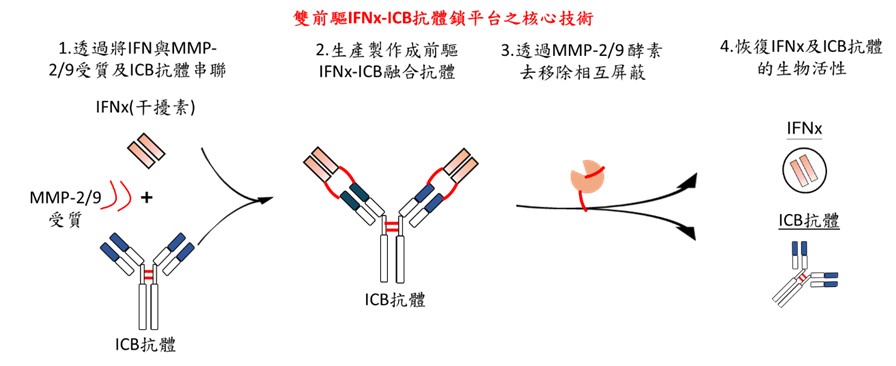
雙前驅IFNx-ICB抗體鎖平台的核心技術在於結合IFN(干擾素)與ICB(免疫檢查點抑制劑)抗體,並利用MMP-2/9酵素的特異性作用,創造出具有雙重功效的前驅融合抗體。這一技術的關鍵在於實現特異性激活,增加療效並減少副作用。以下是技術的詳細描述:首先,IFNx-ICB融合抗體結合了IFN和ICB抗體的優點。IFN能夠促進免疫細胞,如T細胞和NK細胞,對腫瘤細胞的攻擊能力;ICB抗體則可以阻斷免疫檢查點蛋白(如PD-1和CTLA-4),解除對免疫系統的抑制,增強抗腫瘤免疫反應。然而,單獨使用這些分子時,常會引起全身性免疫激活,導致嚴重的副作用。為了解決這一問題,IFNx-ICB融合抗體採用了MMP-2/9酵素敏感的設計。MMP-2/9是腫瘤微環境中特異性高表達的酵素,能夠識別並切割特定的蛋白質序列。通過在IFN和ICB抗體之間引入MMP-2/9酵素的靶位序列,融合抗體在血液中保持非活性狀態,不會引發全身性免疫反應。當融合抗體到達腫瘤微環境時,MMP-2/9酵素特異性地切割靶位序列,去除相互屏蔽,從而釋放IFN和ICB抗體的生物活性。這一過程使得抗體僅在腫瘤區域特異性激活,增強局部的免疫反應,提高療效,同時大幅降低全身性副作用的風險。
功能驗證與動物實驗結果
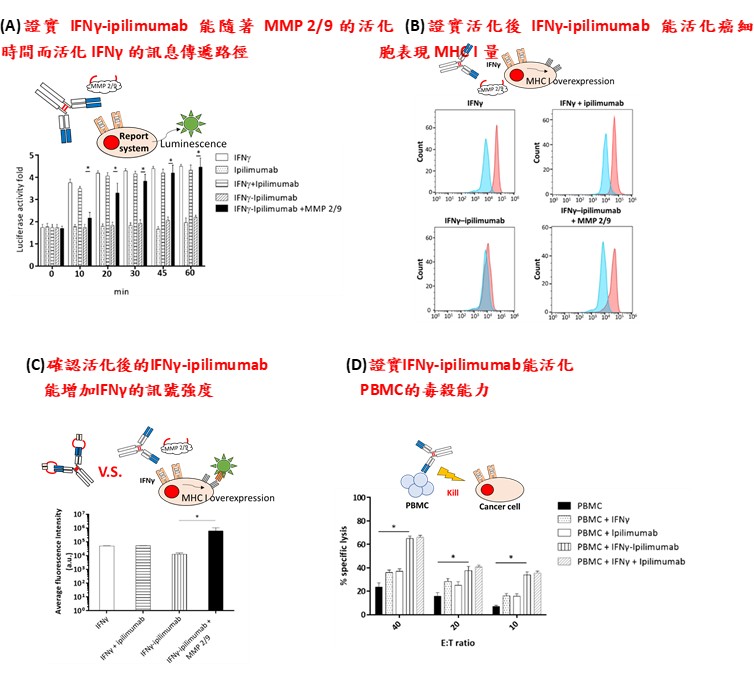
在功能驗證中,我們發現經MMP-2/9處理後的IFNγ-Yervoy能顯著提高SW480腫瘤細胞的MHC I表達,並且顯著提高**外周血單核細胞(PBMCs)**的細胞毒性。無論在任何效應細胞與靶細胞比例(E:T 比)下,其效果都非常突出。
進一步的動物實驗也證實了這種抗體的潛力。在腫瘤異種移植小鼠模型中,我們將小鼠分成幾個組別,進行不同的治療處理,包括PBS對照組、單獨使用的IFNγ與Yervoy組,以及IFNγ-Yervoy融合抗體或兩者組合的治療組。實驗結果顯示,IFNγ-Yervoy不僅能顯著抑制腫瘤生長,還能有效提升腫瘤內CD4+與CD8+ T細胞的浸潤程度,同時增加腫瘤細胞中MHC I分子的表現。此外,腫瘤浸潤淋巴細胞的數量與比例也顯著提升,包括**CD4+/Foxp3+、CD8+/Foxp3+與CD16+**細胞族群,顯示其能夠有效重塑腫瘤微環境,增強抗腫瘤免疫反應。
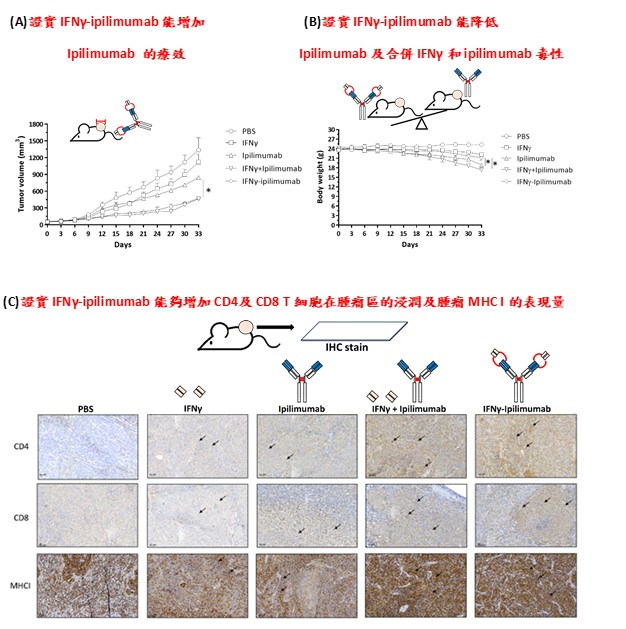
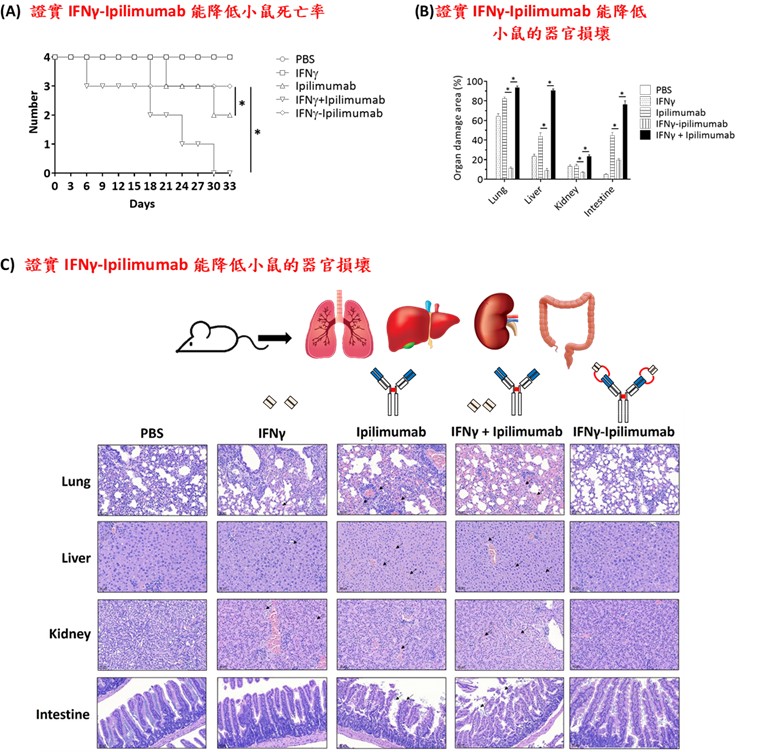
更值得注意的是,這種抗體在安全性方面的表現也相當出色。在小鼠的存活率追蹤與評估肝腎功能相關的生化指標(如GOT、GPT與肌酐)測試中,我們發現接受IFNγ-Yervoy治療的小鼠並未出現明顯的毒性反應或器官損傷,顯示其具有良好的治療耐受性與低毒性風險,具備臨床應用的潛力。
成果與前景
莊智弘副教授與新藥開發暨價創研究中心的研究團隊共同發表了題為「Selective activation of IFNγ–ipilimumab enhances the therapeutic effect and safety of ipilimumab」的研究論文,該論文於2024年6月刊登在《International Journal of Biological Macromolecules》期刊上。這篇期刊的影響因子為8.2,並在應用化學 (CHEMISTRY, APPLIED) 領域中排名前8.10%。並申請了美國臨時專利(111028-US-PRO)與PCT專利優先權。此外,我們的研究還榮獲了第21屆國家新創獎學研獎的肯定,這項研究的重要性在於其揭示了IFNγ與ipilimumab選擇性激活後,能顯著提升ipilimumab的治療效果和安全性,為未來的癌症免疫治療提供了新的方向和更安全的選擇。研究刊登於高影響力的期刊,進一步強調了其在科學界的價值和影響力。

研究聯繫Email:a4132600@gmail.com
論文出處:Selective activation of IFNγ-ipilimumab enhances the therapeutic effect and safety of ipilimumab. Int J Biol Macromol. 2024 Apr;265(Pt 2):130945.
